近期,北京医疗器械创新领域喜讯连连。两款首创医疗器械相继获得国家药品监督管理局上市批准:分别为超目科技研发的全球首创先天性眼球震颤治疗器械——i-NYS植入式眼部肌肉神经刺激器,阿迈特医疗自主研发的国内同品种首个三类二氧化碳造影压力注射套装。两大创新成果接连落地,彰显出首都在高端医械研发与临床转化的硬核实力。
作为全球首款用于先天性眼球震颤治疗的三类有源植入式医疗器械,i-NYS一举填补了这一眼科“不治之症”的治疗空白。据悉,先天性眼球震颤是一种先天遗传性眼疾,发生于出生时或出生时6个月内,通常伴随终身,病症为眼球不自主的节律性跳动或摆动,常导致视力下降、双眼视功能障碍及异常头位,在我国患者数量约130万人。
此次获批的i-NYS,给眼部肌肉和相关神经装上了“精准电刺激调节器”,通过设定专属的电流参数,对眼肌进行个体化的轻微电刺激干预,让不自主跳动、摆动的眼球恢复平稳。该产品源自北大人民医院王乐今教授团队二十余年的潜心攻关,首次将神经电刺激技术应用于先天性眼球震颤治疗领域,并创立超目科技将这一科研成果落地转化。临床试验显示,71例入组受试者在术后黄斑中心凹注视时间提升587%,眼球震颤的幅度、频率分别下降84.1%和79.4%,且均未发生手术相关不良事件。该产品不仅入选国家药监局创新医疗器械“绿色通道”,还获美国食品药品监督管理局(FDA)的人道主义使用器械认定。
阿迈特医疗自主研发的二氧化碳造影压力注射套装获批上市则实现了国内外周介入领域的关键技术突破。这一创新医疗器械把血管造影的“造影剂”从传统含碘液体换成了二氧化碳气体,还搭配了专用的自动化注射设备,从而解决了碘过敏、肾功能不全、甲状腺功能亢进等人群的造影诊疗难题。国内多中心临床研究显示,适用人群的造影剂肾病及严重不良事件发生率均为0%,大幅提升了血管造影的安全性。这款产品已提前完成全球化布局,先后斩获欧盟CE-MDR认证、美国FDA上市备案,目前已在全球20余个国家和地区获批销售,正式开启全球血管造影“零碘”新时代。
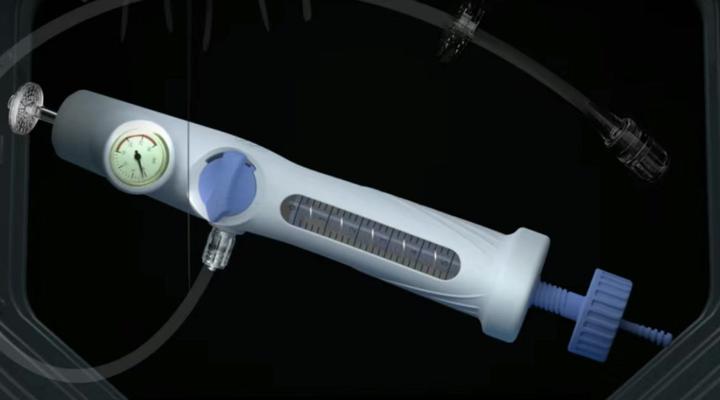
阿迈特研发的二氧化碳造影压力注射套装。来源:阿迈特
两款首创医疗器械的成功落地,是北京医疗器械产业创新生态持续优化的生动缩影。依托未来科学城生命谷、大兴生物医药产业基地等核心产业高地,北京搭建起覆盖研发攻关、临床转化、海外布局的全链条创新服务平台,叠加创新医疗器械“绿色通道”等政策支持,为企业创新发展保驾护航。目前,北京已累计获批国家创新医疗器械84个、手术机器人43个、人工智能医疗器械60个,数量均居全国第一。








